|
来源:医脉通
发表于柳叶刀杂志上的文章从目前现状和未来发展综述了大环内酯类药物在哮喘治疗中的地位,小编整理如下:
前言
大环内酯类是使用最广泛的的抗生素之一,其治疗慢性呼吸疾病范围较广,其中包括囊性纤维化,非囊性纤维化支气管扩张以及慢阻肺(COPD)。
对于具有慢性气道炎症和支气管高反应的哮喘而言,大环内酯类是及有吸引性的治疗选择。慢性哮喘经常合并急性加重,而急性加重大多是由呼吸道病毒感染诱发。鉴于大环内酯类的免疫调节和潜在的抗病毒特性,其治疗哮喘可获益。另外,大环内酯类可广谱覆盖包括非典型肺炎支原体和肺炎衣原体在内的呼吸道病原体,而肺炎支原体和肺炎衣原体均与慢性哮喘和急性发作相关。
大环内酯类具有一个至少12种元素组成的大的内酯环,通过对环的大小和结构进行更改,可获得不同特性的药物。例如,红霉素,克拉霉素,罗红霉素和醋竹桃霉素含有14元环,而阿奇霉素含有15元环。此结构的微妙改变产生了新的大环内酯类,特别是阿奇霉素,生物利用度,酸稳定性和半衰期(40-68 h)均得到改善。酮内酯,如泰利霉素,衍生自阿奇霉素且结构与大环内酯类相似;与其它大环内酯类相比,酮内酯有两个细菌核糖体结合位点,可较好的抵抗对大环内酯类耐药的病原体。
使用大环内酯类治疗哮喘的科学依据可能具有说服力,但其临床试验疗效却存在差异性,可能因为很多研究存在不足。虽然近期的一项荟萃分析显示使用大环内酯类3周或以上可改善呼气风流速,临床症状,生活质量和气道高反应性,但2005年的一项Cochrane数据系统分析结果是不确定的。然而,抗生素的耐药风险和长期使用大环内酯类的不良反应必须纳入考虑。
虽然目前使用大环内酯类治疗哮喘难以评判,但似乎有理由对其保持谨慎乐观的态度。哮喘是一种具有不同表型和亚型的异质综合征。大环内酯类可有效治疗某些表型患者。最近的一项研究显示,阿奇霉素治疗可显着减少严重嗜中性粒细胞性哮喘亚组患者病情急性加重频率,虽然获益机制尚不清楚。但此研究的主要终点是在26周治疗期间的病情急性加重频率。通常FEV1被视为主要衡量结果,而急性加重频率可能更具有临床和经济学意义。
此篇综述,我们评估慢性哮喘和急性加重的临床试验证据,并讨论大环内酯类的科学价值以及与哮喘病理生理的相关性。最后,还讨论大环内酯类治疗的潜在危险,未来研究发展和其治疗哮喘的临床方向。
临床研究:矛盾的证据
在20世纪中叶,口服糖皮质激素广泛用于维持和抢救治疗,被认为可改善中重度哮喘管理。但此改善需以皮质激素产生的副作用为代价,因此被迫寻求节制激素疗法研究。
1958年,Kaplan 和Goldin报道醋竹桃霉素可减少因频繁感染导致急性加重的哮喘患者的咳痰量和激素使用量,其它研究也显示相似的节制激素效果。醋竹桃霉素还可抑制甲基强的松龙清除,可进一步增强节制激素。但在泼尼松龙中未见此疗效。
虽然长期大环内酯类治疗可降低重度哮喘患者口服糖皮质激素维持使用剂量,但对肝毒性的忧虑限制了其广泛使用。吸入性糖皮质激素的使用极大的降低了口服糖皮质激素对哮喘维持治疗的剂量,因此临床研究的重点从节制激素疗法转向辅助疗法。
哮喘临床研究采用一系列测量方法定量评估大环内酯类疗效并确定是否某些疾病特征可更好的对大环内酯类产生反应。但这些结果存在矛盾性,并可能与多种因素相关。
哮喘表型
哮喘的异质性可引起患者不同的自然史和治疗反应,因此大环内酯类治疗不可能对所有表型患者均有效。不同哮喘表型的联合分析会部分解释临床研究中模凌两可的结果。由于COPD的产生和病理生理也有异质性,因此在分析COPD研究时也会遇到此问题。
嗜中性粒细胞性哮喘较其它哮喘亚型对大环内酯类治疗响应更佳;此类患者的特点是气道中最丰富的粒细胞是中性粒细胞,对吸入糖皮质激素等常规疗法响应较差,且多见于重度哮喘患者。
Brusselle及其同事报道,与安慰剂相比,阿奇霉素可显着降低重度嗜中性粒细胞性哮喘患者急性加重频率,但对所有患者进行综合分析时,此获益消失。此作用机制尚不清楚,可能与大环内酯类的抗菌作用和免疫调节作用相关。嗜中性粒细胞性哮喘与细菌负荷和白细胞介素8增加相关。Simpson及其同事的研究显示,克拉霉素治疗显着减少重度哮喘患者痰液中白细胞介素8浓度和中性粒细胞数目。此疗效首先在弥漫性泛细支气管炎中发现,在此疾病中中性粒细胞性炎症发挥关键作用。
慢性非典型病原体感染
众多研究探讨慢性肺炎衣原体或肺炎支原体感染是否对大环内酯类治疗有更好反应,但结果并不相符。
Kraft及其同事报道,克拉霉素治疗经 PCR证实的上部和下部呼吸道样本感染肺炎衣原体或肺炎支原体的哮喘者,可显着增加其FEV1。但Sutherland及其同事未重现类似结果,且克拉霉素显着改善PCR阴性组患者的气道高反应性。此对立性结果可能与慢性非典型病原体感染的难以准确诊断相关。血清学和PCR的联合是检测非典型病原体感染的金标准。由于病原体培养灵敏性较低,血清学和PCR的灵敏性可变,因此两个研究中虽然使用相似的样本和PCR技术,但PCR检测出的肺炎支原体和肺炎衣原体的感染率不同。
疾病严重程度和症状控制
哮喘严重程度的评估主要基于患者治疗前的临床症状和达到充分的控制症状所使用的最低药物剂量。
大环内酯类似乎可有效治疗症状难以控制的重度嗜中性粒细胞性哮喘。相反,对于基线时吸入高剂量糖皮质激素即可控制症状的中至重度哮喘儿童,不能从大环内酯类治疗中获益。同样,对于基线时吸入低剂量糖皮质激素控制症状不佳的吸烟的嗜中性粒细胞哮喘患者,使用大环内酯类治疗后症状无显着改善。
研究者认为,大环内酯类短期治疗(12周)可能是造成此差异的原因。但是,症状未充分控制的轻至中度哮喘患者在增加额外治疗前应吸入高剂量糖皮质激素以进行优化,主要是因为吸入糖皮质激素联合或未联合长效β受体激动剂均可改善症状和肺功能并减少急性加重风险。另外,对于哮喘症状已控制的患者而言,很难检测某种临床症状的显着改善。
治疗方案,疗程和随访期
呼吸科和其它医学专科的证据均表明每日1次用药方案可较好的改善症状。阿奇霉素每日1次用药方案似乎最适宜哮喘患者。此治疗方案也可有效的治疗COPD和社区获得性肺炎,但最佳治疗疗程仍未知。大环内酯类治疗疗程需达3个月可见显着疗效,短期研究在观察到全获益前可能已经终止了。但疗程不是决定结果的唯一因素。一些短期研究(≤8周)已经显示出阳性结果,而其它一些长疗程研究未显示改善结果。大环内酯类的获益似乎也依赖于剂量和给药时间段。
Black及其同事报告了一项大型、多中心研究结果,罗红霉素治疗6个月后,可改善呼气峰流速,Simpson及其同事报告停止使用克拉霉素后,哮喘生活质量问卷(AQLQ)恶化。这些研究结果说明,在大环内酯类剂量足量时延长治疗可能达到所需的全获益,但必须平衡耐药风险和潜在的不良事件。
预后的衡量
对于肺功能,一项meta分析显示,大环内酯类治疗3周或以上未改善FEV1,但呼气峰流速显着改善。此结论是主要基于Black及其同事的研究,即罗红霉素显着增加夜间呼气峰流速。与基线时相比较,罗红霉素组和安慰剂组患者的平均夜间呼气峰流速增加值分别为15 L/min 和3 L/min .虽然具有显着改善,但此改善的临床疗效尚不清楚。另外,肺功能是评估哮喘的有效客观衡量指标,可显示支气管收缩的程度,但用于哮喘其它症状如咳嗽的评估有限,并且与疾病控制的其它衡量指标相关性较差。因此,预后的衡量指标除肺功能外,在评估治疗全效中发挥重要作用。
哮喘的控制采用ACQ进行衡量,肺功能采用AQLQ进行衡量,两者是验证的评估技术,可大体了解患者健康状况。但各研究使用的症状评分系统存在异质性,虽然问题大致相似,但一些研究使用了未经验证的评分系统。虽然结果无统一阳性,但如以上两个meta分析显示,大环内酯类治疗可改善哮喘症状。
与肺炎支原体和肺炎衣原体感染相比,基线时痰液中中性粒细胞和嗜酸性粒细胞计数似乎是治疗反应的最好指标,虽然这一结果仍需验证。几个临床研究显示,大环内酯类显着降低嗜中性粒细胞和嗜酸性粒细胞计数以及促炎细胞因子浓度。一项研究显示,停止大环内酯类治疗后,白细胞介素 8 和痰液中的中性粒细胞计数增加。迄今为止,无生物标志物可有效监测疗效。
急性加重
大环内酯类治疗哮喘急性发作疗效的数据非常少。
大环内酯类的免疫调节特性
大环内酯类具有独立于抗菌活性的免疫调节作用。虽然在临床和动物研究中可见这些疗效,但主要是在体外细胞培养系统中研究。此次我们回顾了大环内酯类与哮喘相关的免疫调节活性。阿奇霉素是最常研究的大环内酯类(如图)。虽然细胞培养和动物研究非常有用,但未显示哮喘表型的复杂性和异质性,因此,对这些研究结果需谨慎解释。
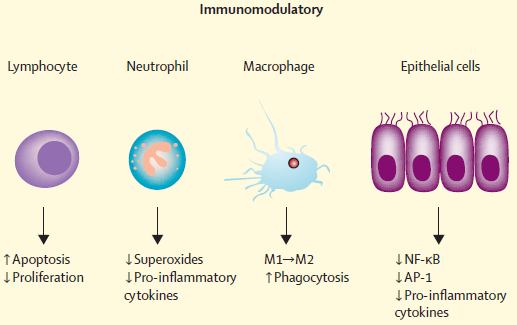

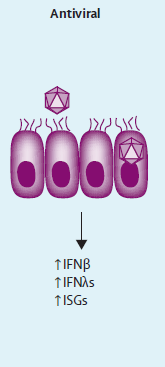
图:大环内酯类药物,特别是阿奇霉素的免疫调节,抗菌,和抗病毒特性的总结。AP-1= 激活蛋白 1.IFN= 干扰素。ISG = 干扰素刺激基因。NF-κB= 核因子 -κB .Th2= 2 型辅助性 T 淋巴细胞。
促炎信号通路的抑制
阿奇霉素可抑制肺上皮细胞中的促炎转录因子如核因子 -κB(NF-κB)和激活蛋白 1(AP1)的活化,因此可调包括胸腺基质淋巴细胞生成素(TSLP),白细胞介素6,白细胞介素 8 等基因。
NF-κB信号通路是先天性免疫和适应性免疫的重要调节因子;其在抗呼吸道病毒感染的先天免疫中发挥关键作用。NF-κB 的活化及其随后形成的炎性复合体可导致促炎性细胞因子,如 TNF-α,白细胞介素 1β和白细胞介素 8等的释放,引发巨噬细胞,树突状细胞,以及中性粒细胞等的募集和活化。
TSLP 可使树突状细胞成为Th2细胞的强诱导物,并导致气道出现嗜酸性粒细胞性炎症、粘膜增生,以及气道高反应。
有研究比较了阿奇霉素和类固醇激素对 NF-κB 活化的抑制作用,结果显示类固醇激素似乎有较好的疗效和潜力。一项对支气管肺发育不良的早产儿气管抽吸物进行的体外研究显示,阿奇霉素可抑制 TNFα诱导的 NF-κB 的活化,以及白细胞介素 6 和白细胞介素 8 的释放。
但另一项研究显示,阿奇霉素具有促炎活性;在治疗的初期,阿奇霉素可增加自发性白细胞介素 8 的释放,以及脂多糖诱导的白细胞介素 8的 释放,尽管这两种白细胞介素 释放水平在治疗5天后均又达到基线浓度(即使使用脂多糖持续刺激)。因此,阿奇霉素对炎症信号途径以及与其相关基因的作用是复杂的,这与磷脂和细胞外信号调节激酶 1 和 2 的相互作用相关。
|